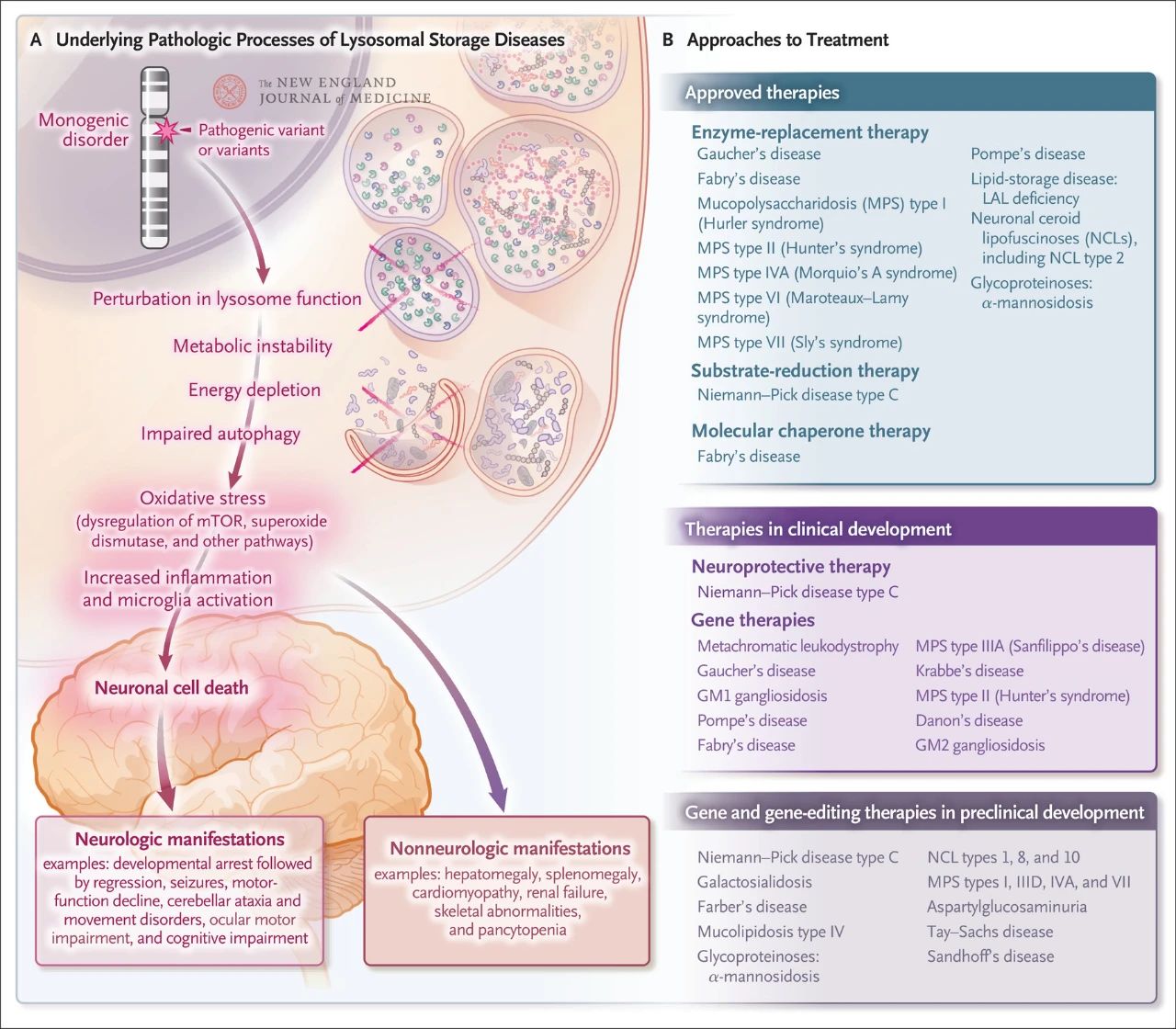
비교적 드물지만, 리소좀 저장 질환의 전체 발병률은 출생아 5,000명당 약 1명입니다. 또한, 알려진 리소좀 저장 질환은 약 70가지이며, 그중 70%는 중추신경계에 영향을 미칩니다. 이러한 단일 유전자 질환은 리소좀 기능 장애를 유발하여 대사 불안정성, 포유류 라파마이신 표적 단백질(mTOR, 일반적으로 염증을 억제함)의 조절 장애, 자가포식 장애, 그리고 신경 세포 사멸을 초래합니다. 효소 대체 요법, 기질 감소 요법, 분자 샤페론 요법, 유전자 요법, 유전자 편집, 신경 보호 요법 등 리소좀 저장 질환의 근본적인 병리학적 기전을 표적으로 하는 여러 치료법이 승인되었거나 개발 중입니다.
니만-픽병 C형은 NPC1(95%) 또는 NPC2(5%)의 이중대립유전자 돌연변이로 인해 발생하는 리소좀 저장 세포 콜레스테롤 수송 질환입니다. 니만-픽병 C형의 증상으로는 유아기의 급속하고 치명적인 신경학적 저하가 있으며, 후기 청소년기, 청소년기, 그리고 성인기에 발병하는 유형으로는 비장비대, 핵상 주시 마비, 소뇌 운동실조, 조음장애, 그리고 진행성 치매가 있습니다.
이번 호 저널에서 Bremova-Ertl 외 연구진은 이중맹검, 위약대조, 교차 임상시험 결과를 보고했습니다. 이 임상시험은 잠재적인 신경보호제인 아미노산 유사체 N-아세틸-L-류신(NALL)을 사용하여 니만-픽 C형 질환을 치료했습니다. 연구진은 증상이 있는 청소년 및 성인 환자 60명을 모집했으며, 그 결과 운동실조 평가 및 평가 척도(Ataxia Assessment and Rating Scale)의 총점(1차 평가변수)에서 유의미한 개선을 보였습니다.
NALL과 n-acetyl-D-leucine의 라세미체인 N-acetyl-DL-leucine(Tanganil)의 임상 시험은 주로 경험에 의한 것으로 보이며, 작용 기전은 명확하게 밝혀지지 않았습니다. N-acetyl-dl-leucine은 1950년대부터 급성 현기증 치료제로 승인되었습니다. 동물 모델에 따르면 이 약물은 내측 전정 신경세포의 과분극과 탈분극을 재조정하여 작용합니다. 이후 Strupp 등은 다양한 원인으로 인한 퇴행성 소뇌 운동실조증 환자 13명의 증상이 개선되는 것을 관찰한 단기 연구 결과를 보고했으며, 이는 이 약물에 대한 재연구에 대한 관심을 다시 불러일으켰습니다.
영어: n-acetyl-DL-leucine이 신경 기능을 개선하는 기전은 아직 명확하지 않지만, Niemann-Pick 병 유형 C와 또 다른 신경 퇴행성 리소좀 질환인 GM2 ganglioside storage disorder 변이 O(Sandhoff 병)의 두 가지 마우스 모델에서 발견된 결과는 NALL에 대한 관심을 불러일으켰습니다. 구체적으로, n-acetyl-DL-leucine 또는 NALL(L-거울상 이성질체)로 치료한 Npc1-/- 마우스의 생존율이 향상되었지만, n-acetyl-D-leucine(D-거울상 이성질체)으로 치료한 마우스의 생존율은 그렇지 않았습니다. 이는 NALL이 이 약물의 활성 형태임을 시사합니다. GM2 ganglioside storage disorder 변이 O(Hexb-/-)에 대한 유사한 연구에서, n-acetyl-DL-leucine은 마우스의 수명을 약간이지만 유의미하게 연장시켰습니다.
연구진은 n-아세틸-DL-류신의 작용 기전을 규명하기 위해 돌연변이 동물의 소뇌 조직에서 대사산물을 측정하여 류신의 대사 경로를 조사했습니다. GM2 강글리오사이드 저장 장애의 변형 O 모델에서, n-아세틸-DL-류신은 포도당과 글루탐산 대사를 정상화하고, 자가포식을 증가시키며, 활성산소 제거효소인 슈퍼옥사이드 디스뮤타제 수치를 증가시킵니다. 니만-픽병의 C 모델에서는 포도당과 항산화 대사의 변화와 미토콘드리아 에너지 대사의 개선이 관찰되었습니다. L-류신은 강력한 mTOR 활성제이지만, 두 마우스 모델 모두에서 n-아세틸-DL-류신 또는 그 거울상 이성질체로 처리한 후 mTOR 수치나 인산화에 변화가 없었습니다.
NALL의 신경 보호 효과는 피질 충돌로 유발된 뇌 손상 마우스 모델에서 관찰되었습니다. 이러한 효과에는 신경 염증 마커 감소, 피질 세포 사멸 감소, 그리고 자가포식 흐름 개선이 포함됩니다. NALL 치료 후, 손상된 마우스의 운동 및 인지 기능이 회복되었고 병변의 크기가 감소했습니다.
중추신경계의 염증 반응은 대부분의 신경퇴행성 리소좀 저장 질환의 특징입니다. NALL 치료를 통해 신경염증을 감소시킬 수 있다면, 모든 신경퇴행성 리소좀 저장 질환은 아니더라도 많은 임상 증상이 호전될 수 있습니다. 이 연구에서 밝혀진 바와 같이, NALL은 리소좀 저장 질환에 대한 다른 치료법과도 시너지 효과를 낼 것으로 예상됩니다.
많은 리소좀 저장 장애 또한 소뇌 운동실조와 관련이 있습니다. GM2 갱글리오사이드 저장 장애(테이-삭스병 및 샌드호프병)를 가진 소아 및 성인을 대상으로 한 국제 연구에 따르면, NALL 치료 후 운동실조가 감소하고 미세 운동 협응력이 개선되었습니다. 그러나 대규모 다기관, 이중맹검, 무작위, 위약 대조 연구에서는 n-아세틸-DL-류신이 혼합형(유전성, 비유전성, 원인 미상의) 소뇌 운동실조 환자에게 임상적으로 효과가 없음을 보여주었습니다. 이 결과는 유전성 소뇌 운동실조 환자를 대상으로 한 임상시험에서만 효능이 관찰될 수 있으며, 관련 작용 기전을 분석해야 함을 시사합니다. 또한, NALL은 외상성 뇌손상으로 이어질 수 있는 신경 염증을 감소시키므로, 외상성 뇌손상 치료를 위한 NALL 임상시험이 고려될 수 있습니다.
게시 시간: 2024년 3월 2일